BoneDiaS-Diagnosesystem
Medizinische Information:Früherkennung von Arthrose im Knie- und Hüftgelenk
Wieso wird Schall aus Gelenken emittiert?
Ursache der Schallemission aus Gelenken sind Reibung zwischen korrespondierenden Gelenkoberflächen und Strömung der Synovialflüssigkeit. Die Emission nimmt zu bei pathologischen Entwicklungen am Gelenkknorpel mit Änderungen in der Kontur der Gelenkoberflächen, mit Zunahme der Oberflächenrauigkeit und auch mit Änderungen in Viskosität und partikulärer Kontamination der Synovialflüssigkeit.
Welche Schäden an Gelenken haben Einfluss auf die Schallemission?
Nicht nur die bekannten, schweren Schäden am Gelenkknorpel wie bei Osteonekrose oder Osteochondritis dissecans, wie in späteren Stadien bei Osteoarthritis mit grossen Knorpel-Defekten, Verschmälerung des Gelenkspaltes, Bildung von Osteophyten und subchondralen Zysten sowie mit subchondraler Sklerose und wie bei Rheumatoider Arthritis, die eine gravierende, erosive Erkrankung ist mit Synovia-Proliferationen sowie schwerer Erosion und Zerstörung des Gelenkknorpels, haben Einfluss auf die Schallemission. Schon früheste Änderungen im Knorpel bei beginnender Osteoarthritis, wie der Verlust von Proteoglykanen und der Abbau des Netzwerks der faserigen Kollagene (Buckwalter and Mankin, 1997), verbunden mit dem Erweichen des Knorpels (Armstrong and Mow, 1982), mit abnehmender Belastungsfähigkeit sowie Rissbildung und Auffaserung im Knorpel (Palmoski and Brandt, 1981) verändern die Schallemissionmission.
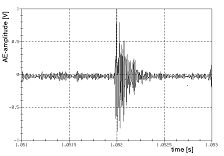
Wie sehen die Schallsignale bei frühen Knorpeländerungen aus?Steifer Knorpel mit hoher Dämpfung wie bei jungen Erwachsenen ist gekennzeichnet durch diskrete Schallereignisse mit steilem Anstieg (kurze „rise time“ des Signals, s. Abbildung 1) und steilem Abfall, erkennbar z. Bsp. beim schnellen Übergang vom Zweibein- zum Einbein-Stand eines jungen Erwachsenen, s. Abbildung 1.
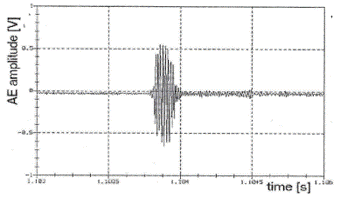
Die bei beginnendem Knorpel-Umbau (frühe Phase) auftretende Erweichung des Knorpels, bei der häufig auch Läsionen auftreten, ist gekennzeichnet durch kontinuierliche Schallemission mit weniger steilen Anstiegen (grosse „rise time“ / hohe Dämpfung) und Abfallen („decay“ groß) der SE-Signale, dem erkennbaren Eintauchen in und Ausgleiten aus Läsionen und durch lange Signaldauer, da neue, schadensbedingte Schallemissionen erfolgen, ohne dass die vorangehende Emission abgeklungen ist, s. Abbildung 2. Mit zunehmender Knorpelveränderung wird auch die schadensbedingte Grundemission immer grösser („threshold“). Die mechanisch umgesetzte Energie im Gelenk ist winkelabhängig unterschiedlich. Dies macht sich in einer unterschiedlich hohen Grundemission bemerkbar, die bei hoher Reib-Energie ebenfalls hoch ist.
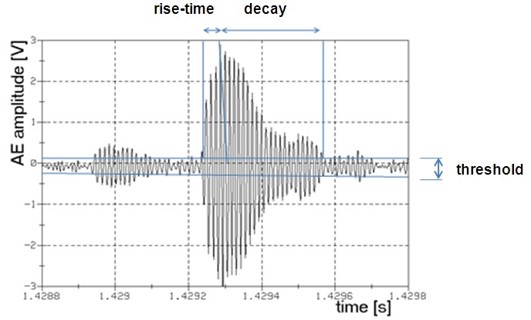
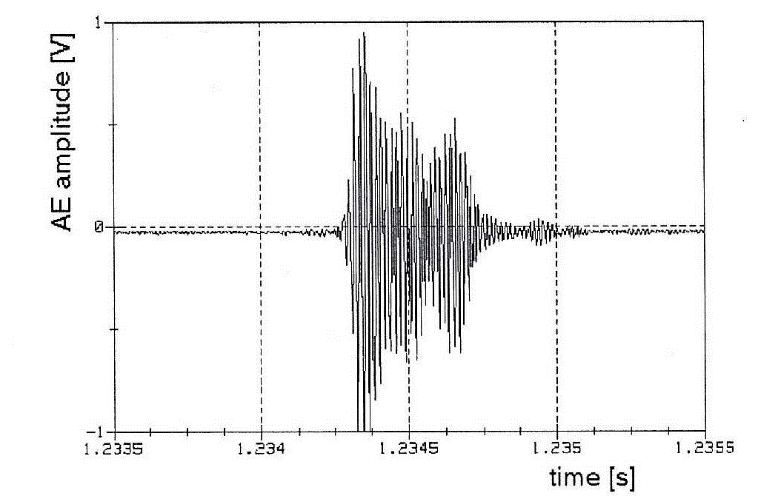
Bei fortgeschrittenem Um- und Abbau des Knorpels in späteren Phasen kommt es immer mehr zur Reibung auch an der subchondralen Grundplatte; es entsteht hierbei knöcherne Festkörperreibung, deren Schallemission durch steigende Signalhäufigkeit gekennzeichnet ist. Die Energie der SE-Signalen nimmt zu und aufgrund abnehmender mechanischer Dämpfung des Knorpels sinkt die rise-time. Wenn Rauhigkeitsspitzen abbrechen, werden diese durch den Gelenkspalt gezogen und verursachen ihrerseits erneut Schallemissionen. So treten während der Abklingdauer eines Ereignisses neue SE-Ereignisse auf, wie auch Abbildung 3 zeigt.
Welchen Einfluss hat eine frühe Diagnose?
Die Rheumatoide Arthritis zeigt: Bei früh einsetzender Behandlung ist für mehr als die Hälfte der Betroffenen eine Beschwerdefreiheit möglich. Bei sehr frühem Therapiebeginn wird rund die Hälfte der Betroffenen vollständig beschwerdefrei. Die ersten drei bis sechs Monate der Erkrankung stellen ein »therapeutisches Fenster« dar, innerhalb dessen der immunologische Prozess gestoppt oder nachhaltig verändert werden kann. Frühe Diagnose und Therapieeinleitung sind von entscheidender Bedeutung für das Schicksal der Betroffenen. Eintritt und Ausmaß der Erkrankung haben enorme volkswirtschaftliche Bedeutung.
Können die bislang eingesetzten Verfahren die frühe Diagnose liefern?
Generell sind Veränderungen im Gelenkknorpel mit Röntgenverfahren nicht direkt darstellbar. Dagegen kann das manchmal mit dem Kernspin-Resonanz-Verfahren gelingen. Frühe Veränderungen im Gelenkknorpel können jedoch mit keinem dieser Verfahren diagnostisch erschlossen werden, wie bei Osteomalazie festgestellt wurde.
Welche Bedeutung hat die Gelenk-Zone der Lastübertragung?
Das wird am Kniegelenk exemplarisch erkennbar: Man bezeichnet die Gelenkbewegungen im Knie als Roll- Gleit-Bewegung. Die im Kniegelenk zwischen Unter- und Oberschenkel übertragene Körperlast wird daher nicht in einem Punkt oder einer einzelnen kleinen Zone übertragen, sondern in einer Vielzahl nacheinander kontaktierender, kleiner Zonen, die zusammen die Lastabtrags-Zone bilden. Insbesondere hier tritt Knorpelverschleiß auf, entweder ganz überwiegend durch Mechanismen, die durch zu ungünstige Lastübertragung hervorgerufen werden oder durch lastbedingte Mechanismen in Kombination mit unfalls-, alters- oder krankheitsbedingten Knorpelschäden.
Die Schallemission aus dieser Lastabtrags-Zone hängt neben der Qualität des Gelenkknorpels und der Synovialflüssigkeit auch von der Intaktheit der Kniegelenksbänder ab.
Zur Prävention von Schäden im Gelenkknorpel muss man also die Lastabtrags-Zone finden und analysieren. Wegen der Abhängigkeit der Lastabtrags-Zone im Kniegelenk vom Winkel zwischen Ober- und Unterschenkel (Roll- Gleit-Bewegung) muss die Analyse daher in kompletten Beugungs- Streckungs- Zyklen der Beine unter alltäglicher Belastung durchgeführt werden. Keines der anderen in der Routine eingesetzten Verfahren zur Erfassung von Schäden im Kniegelenksknorpel (z. Bsp. Endoskopische Arthroskopie, MRT, CT) ist in der Lage, Untersuchungen am Kniegelenk unter komplettem Bewegungszyklus und unter alltäglicher Belastung durchzuführen. Darüber hinaus werden mit diesen Verfahren auch nicht die frühen Schäden am Gelenkknorpel erfasst.
Die Schallemissionsanalyse (SEA) besitzt also zwei Alleinstellungsmerkmale. Sie
- erkennt die aktive Lastabtrags-Zone und Schäden in ihr und sie .
- charakterisiert frühe Schädigungen im Gelenkknorpel.
Wie wird das BoneDiaS-System verwendet?
Nur das piezoelektrische Sensorelement zur Erfassung der Schallemission ist im Kontakt mit der Haut, die direkt darunterliegende Knochen bedeckt, z.B. prominente Anteile des Femurs wie die Kondylen. Zwischen Sensor und Haut werden ein Gel mit Zulassung zum klinischen Gebrauch in der Ultraschall-Analytik zur akustischen Ankopplung und ein Wachs, das im Theater für die Make up- Routine eingesetzt wird, zum Abdichten der Saugglocke verwendet. Mit Hilfe der Saugglocke mit definiertem Unterdruck wird eine reproduzierbare Anpressung des Sensors an die Haut gewährleistet. Alle anderen Bestandteile des Systems befinden sich in einer Mess-Box, die am Oberschenkel befestigt wird (Abbildung 4). Das gesamte System wird nicht-sterilisiert verwendet, wobei der piezoelektrische Sensor vor jeder Anwendung sorgfältig gesäubert wird. Das System enthält keine pharmakologisch wirksamen Substanzen.
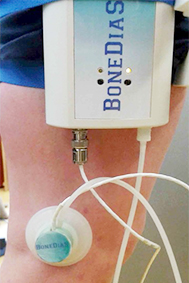
Der piezoelektrische Sensor befindet sich in Abbildung 4 am lateralen Kondylus des rechten Oberschenkels und die Mess-Box am rechten Oberschenkel eines Probanden.
Das SEA-basierte BoneDiaS-System wird angesichts des Leistungs-Profils der SEA mit hohem Nutzen und ohne Risiken vom Markt aufgenommen.
ReferencesBuckwalter JA, Mankin HJ. Articular cartilage: degeneration and osteoarthritis, repair, regeneration, and transplantation. Instr Course Lect. 1998;47:487-504.
Armstrong CG, Mow VC. Variations in the intrinsic mechanical properties of human articular cartilage with age, degeneration, and water content. J Bone Joint Surg Am. 1982 Jan;64(1):88-94.
Palmoski MJ, Brandt KD. Proteoglycan depletion, rather than fibrillation, determines the effects of salicylate and indomethacin on osteoarthritic cartilage. Arthritis Rheum. 1985 May;28(5):548-53.
Bestimmung der Rissbildungsgrenze im menschlichen Femur und dessen Belastungsgrenze bei gezieltem therapeutischen Training
Die prinzipielle Frage der Bewertung der Rissbildungsgrenze des menschlichen Knochens nach einem Knochenbruch oder bei osteoporotischer Erkrankung ist weniger die Frage gezielt Mikrorisse zu erzeugen, als vielmehr die Frage wie verändert sich die Rissbildungsgrenze des Knochens mit dem Heilungsprozess oder dem Verlauf der Erkrankung. Zur Diagnose des Bruchverhaltens des menschlichen Femurs sind Bewegungen und mechanische Belastungen erforderlich. Diese Bewegungen und Belastungen entsprechen den täglichen natürlichen Beanspruchungen des menschlichen Stützapparates – Aufstehen von einem Stuhl, Kniebeuge, Treppen auf- oder absteigen u. a. - und gelten unter Orthopäden als zerstörungsfreie Belastungen, obwohl bereits in der Mikrostruktur Risse in der Grenzschicht Compacta-Spongiosa auftreten, die für den physiologischen Knochenumbau unerlässlich sind. Zur Bewertung veränderlicher Knochenfestigkeit ist ausschließlich die Bestimmung der Rissbildungsgrenze erforderlich.
Zur Beurteilung der Risszähigkeit des Femurs sind weitergehende Untersuchungen zur Rissbildung und des Rissfortschrittes notwendig, die eine bruchmechanische Bewertung mit einschließt. Diese Untersuchungen können in-vivo durchgeführt werden.